Transplante de células-tronco hematopoiéticas (TCTH)
O transplante alogênico de células tronco
(infusão de células-tronco de um doador em um paciente) é uma opção para
alguns pacientes de LMC. É o tratamento curativo para eles. Esse tipo
de transplante, entretanto, pode causar sérios, ou até fatais,
complicações e efeitos colaterais, e normalmente não é uma boa opção para pacientes mais velhos ou pacientes com outros problemas de saúde. Os resultados são muito semelhantes se o doador compatível for um parente ou uma
pessoa sem parentesco.
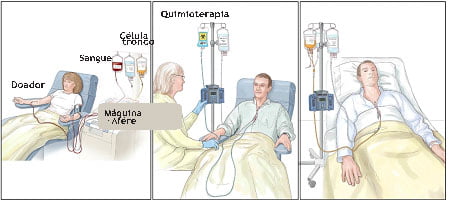
Foto 1: Células-tronco são coletadas do doador
Foto 2: Paciente recebe tratamento quimioterápico para destruir as células doentes
Foto 3: Paciente recebe as células-tronco do doador
A opção pelo transplante alogênico é cada vez mais rara porque muitos pacientes têm uma resposta muito boa aos inibidores de tirosina quinase, controlando a doença por um longo período e preservando a qualidade de vida sem os sérios riscos do transplante.
O médico irá considerar muitos fatores importantes ao decidir se o transplante alogênico é a melhor escolha de tratamento para um paciente. Esses fatores incluem a idade do paciente, saúde em geral, a fase da LMC, a resposta a outros tratamentos e a disponibilidade de um doador compatível. O transplante é considerado no caso de pacientes que tenham resistência a, pelo menos, dois tipos de inibidores de tirosina quinase; para pacientes que a LMC esteja na fase acelerada ou blástica e para pacientes que sejam intolerantes a todos os tipos de inibidores de tirosina quinase.
O fator prognóstico mais importante para a sobrevida após o transplante é a fase da LMC. Aproximadamente 90% dos pacientes com LMC crônica estarão livres da doença por 5 anos. Já os pacientes com LMC acelerada, de 40 a 50% deles estarão livres da doença após 5 anos e, apenas 10 a 20% dos pacientes com LMC blástica estarão livres da doença após 5 anos.
Cada fase da LMC requer um tipo diferente de tratamento.
A terapia com inibidores da tirosina quinase é padrão para a LMC na fase crônica pois a resposta ao tratamento é boa por longos períodos de tempo.
Três tipos de inibidores da tirosina quinase estão aprovados no Brasil para o tratamento primário para LMC fase crônica. Eles são:
– Imatinibe 400 mg uma vez ao dia
– Dasatinibe 100 mg uma vez ao dia
– Nilotinibe 300 mg duas vezes ao dia
Ao escolher um inibidor de primeira linha, os médicos devem considerar fatores como condições de saúde pré-existentes, idade, pontuação de risco, cronograma de dose e custo. Depois de iniciada a terapia, o médico irá monitorar o paciente para determinar quão bem ele está respondendo ao tratamento. Um paciente que estiver respondendo bem, continuará com o seu tratamento atual. Se o paciente não estiver correspondendo às expectativas, o médico precisará descobrir o porquê.
Uma análise de mutação genética deve ser realizada para investigar as mutações no gene BCR-ABL. O médico também analisará se o paciente está ou não aderindo ao plano de tratamento. Se o tratamento atual não estiver funcionando, existem várias outras opções. Elas incluem:
– Alertar aos pacientes que não estão tomando a medicação como prescrita sobre a importância da adesão consciente ao tratamento
– Aumentar a dose do medicamento (se possível)
– Trocar por outro inibidor da tirosina quinase. Por exemplo, trocar o imatinibe pelo dasatinibe ou nilotinibe.
– Tentar quimioterapia
– Avaliar se o transplante alogênico de células-tronco é uma opção
O tratamento da LMC na fase acelerada tem como objetivo eliminar todas as células que contenham o gene BCR-ABL, levando à remissão. Se isso não for possível, o objetivo é fazer a doença regredir à fase crônica. Realizar o tratamento em um centro especializado, com médicos que tenham experiência em tratar essa patologia, é recomendado para pacientes que estejam na fase acelerada.
Na fase acelerada da LMC, as células do câncer normalmente adquirem novas mutações genéticas que podem fazer com que os tratamentos sejam menos efetivos. Os pacientes devem passar pela análise da mutação do gene BCR-ABL antes de começar o tratamento para determinar qual opção de tratamento é melhor.
As opções de tratamento para a fase acelerada da LMC dependem dos tratamentos anteriores do paciente. Se a LMC for diagnosticada na fase acelerada e o paciente ainda não tentou um inibidor de tirosina quinase, uma das opções é tentar essa terapia. Isso inclui:
– Tomar Imatinibe 600 mg uma vez ao dia, ou
– Tomar Dasatinibe 140 mg uma vez ao dia, ou
– Tomar Nilotinibe 400 mg duas vezes ao dia
Se a LMC passar da fase crônica para a fase acelerada durante o tratamento com a terapia de inibidor da tirosina quinase, o paciente pode tentar aumentar a dose inicial (se possível) trocar por outro inibidor que ainda não tenha sido tentado. Outras opções incluem:
– O inibidor ponatinibe para pacientes que não tenham respondido a dois ou mais inibidores e que tenham a mutação T315I
– Transplante alogênico de células-tronco
Outra opção para pacientes com LMC acelerada é se submeter a um tratamento experimental, em estudo clínico – uma pesquisa feita por médicos para avaliar novos medicamentos ou novos usos para medicamentos já aprovados para outros casos. Estudos clínicos são um meio do paciente conseguir o mais novo tratamento para câncer. O objetivo da pesquisa clínica para LMC é melhorar o tratamento, melhorar a qualidade de vida e achar a cura.
Os pacientes devem discutir com o médico os possíveis benefícios e riscos de participar em um ensaio clínico.
Sobre o tratamento da fase blástica da LMC:
Pacientes com LMC blástica têm um número maior de blastos. A doença na fase blástica age como uma leucemia aguda, com uma contagem de células do sangue mais alta e sintomas mais graves. É recomendado que o paciente se trate em um local especializado, com médicos que tenham expertise com pacientes de LMC em fase blástica.
É preciso fazer dois importantes testes antes de iniciar o tratamento para a LMC blástica. O primeiro teste determina se a fase blástica envolve blastos mieloides ou linfoides. Esse exame é necessário porque o tipo de célula define o tratamento. O segundo teste, uma análise da mutação do gene BCR-ABL, procura por mutações na parte BCR-ABL do gene que produz a proteína BCRABL.
Diferentes mutações podem fazer a proteína BCR-ABL mais ou menos resistente aos inibidores de tirosina quinase. Uma opção para os pacientes com LMC blástica é receber o tratamento em um estudo clínico. Os pacientes devem discutir com o médico os benefícios e riscos de participar de um estudo clínico.
Outra opção de tratamento é receber os inibidores de tirosina quinase, com ou sem quimioterapia, e depois fazer o transplante alogênico de células-tronco. No geral, na fase blástica da LMC é preferível usar inibidores de segunda geração porque são mais potentes.
Mesmo respondendo à essa terapia, os pacientes podem precisar do transplante alogênico de células-tronco. O resultado do transplante alogênico de células-tronco tem mais chance de ser bem-sucedido quando se consegue regredir da fase blástica para a fase crônica antes do transplante.
INDICE DE RESPOSTA
MEDINDO A RESPOSTA AO TRATAMENTO DA LMC
Após o início do tratamento o seu médico irá pedir, periodicamente, exames de sangue e medula óssea para determinar a sua resposta ao tratamento. Monitorar essa resposta é uma das estratégias chaves para administrar a LMC. Em geral, quanto melhor a resposta ao medicamento, mais tempo a doença ficará controlada.
A tabela 2 mostra os diferentes tipos de respostas ao tratamento.
Existem três tipos de respostas: hematológica, citogenética e molecular.
RESPOSTA HEMATOLÓGICA
Essa resposta é classificada como “parcial” ou “completa” dependendo dos resultados dos hemogramas. Esse exame mede a quantidade de glóbulos brancos, glóbulos vermelhos e plaquetas no sangue.
Resposta hematológica parcial
Os valores de cada tipo de células do sangue começam a voltar ao normal.
Resposta hematológica completa
Os valores das células do sangue voltam ao normal.
A maioria dos pacientes sob tratamento com os inibidores de tirosina quinase tem uma resposta hematológica completa dentro de três meses desde o começo do tratamento.
RESPOSTA CITOGENÉTICA
Avalia o número de células na medula óssea que contém o cromossomo Ph. Tanto o teste citogenético quanto o FISH podem ser usados para fazer essa medição.
Resposta citogenética completa
Nenhuma célula com o cromossomo Ph é detectada na medula óssea
Resposta citogenética parcial
O cromossomo Ph é achado em 1 a 35% das células
Resposta citogenética maior
O cromossomo Ph é achado em mais de 35% das células da medula óssea.
A citogenética da medula óssea é avaliada na consulta de acompanhamento de 3 e de 6 meses para verificar a resposta do paciente ao tratamento se o PCR não estiver disponível.
RESPOSTA MOLECULAR
A resposta molecular avalia a diminuição na quantidade de células com o gene BCR-ABL. O teste PCR conta o número de células no sangue periférico que contém o gene BCR-ABL. A resposta molecular inicial do paciente ao tratamento é importante para prever o resultado e para determinar as futuras opções de tratamento.
Resposta molecular precoce
Quando o nível do gene BCR-ABL é menor do que 10% no 3º e no 6º mês após o início do tratamento; significa que menos de 10% das células (10 a cada 100 células) têm o gene BCR-ABL.
Resposta molecular maior
Quando o nível do gene BCR-ABL é menor do que 0,1%; significa que 1 a cada 1.000 células têm o gene BCR-ABL, conhecido como “redução de 3 logs”.
Resposta molecular completa
Quando nenhuma célula tem o gene BCRABL, também conhecido como “resposta molecular profunda”.
ESCALA INTERNACIONAL, MEDIÇÃO DE TESTE DE PCR
É uma escala padrão para medir os resultados do teste PCR, isto é, medir o número de células que têm o gene BCR-ABL e determinar quão bem o tratamento está funcionando. A Escala Internacional define a linha de base padrão como BCR-ABL 100%. Uma redução de log indica que o nível de BCR-ABL diminuiu uma certa quantidade a partir da linha de base padrão.
– Redução de 1 log indica que o nível do BCR-ABL diminuiu 10 vezes abaixo da linha de base padrão. Isso significa que 10% das células (10 a cada 100 células) têm o gene BCR-ABL, também conhecido como “BCR-ABL 10%”. Essa redução é equivalente a resposta molecular precoce.
– Redução de 2 log significa que o nível de BCR-ABL diminui 100 vezes abaixo da linha padrão. Isso significa que 1% das células (1 a cada 100 células) têm o gene BCR-ABL, também conhecido como “BCR-ABL 1%”.
– Redução de 3 log significa que BCR-ABL diminuiu 1.000 vezes abaixo da linha padrão. Isso significa que 0,1% das células (1 a cada 1.000 células) têm o gene BCR-ABL, também conhecido como “resposta molecular maior”.
– Redução de 4,5 log significa que 0,0032% das células tem o gene BCR-ABL. Redução de 4,5 log é chamado de “resposta molecular completa” ou “resposta molecular profunda”. Alcançar a resposta molecular profunda é um sinal de que a doença está em remissão. Pacientes que alcançam e mantêm a resposta molecular profunda por um período significativo de tempo podem ser considerados como candidatos para descontinuar o medicamento em um estudo clínico.
O teste de PCR pode não estar padronizado entre os laboratórios, uma vez que estes estabelecem seus próprios padrões. Consequentemente, uma mesma amostra pode apresentar resultados diferentes se analisada em laboratórios distintos. Assim, para obter resultados mais consistentes, é melhor fazer os testes sempre no mesmo lugar. Isso ajudará os pacientes e a sua equipe de saúde a monitorarem com mais eficácia as respostas ao tratamento. É recomendado realizar o teste de PCR a cada três meses nos dois primeiros anos. Após dois anos, se o paciente estiver apresentando uma resposta ao tratamento satisfatória, o teste poderá ser feito a cada três ou seis meses.
obs. conteúdo meramente informativo procure seu médico
abs
Carla
https://www.abrale.org.br/




Nenhum comentário:
Postar um comentário
Vc é muito importante para mim, gostaria muito de saber quem é vc, e sua opinião sobre o meu blog,
bjs, Carla